jueves, 31 de marzo de 2016
martes, 15 de marzo de 2016
La velocidad
La velocidad es una magnitud física de carácter vectorial que expresa la distancia recorrida de una unidad de tiempo.
La unidad de velocidad en el (Sistema Internacional) es el metro por segundo: m/s
También se utiliza mucho otra unidad: el km/h
La fórmula para poder escribir expresiones que nos sirvan para cualquier caso utilizando el lenguaje algebraico.

La unidad de velocidad en el (Sistema Internacional) es el metro por segundo: m/s
También se utiliza mucho otra unidad: el km/h
La fórmula para poder escribir expresiones que nos sirvan para cualquier caso utilizando el lenguaje algebraico.
viernes, 11 de marzo de 2016
jueves, 10 de marzo de 2016
Modelos atómicos
Hay 6 tipos de modelos atómicos:
1.- Modelo atómico de John Dalton (1808)
Este modelo te explicaban como se combinaban las sustancias entre sí.
También te explicaba que aún habiendo distintos tipos de sustancias estas se podían explicar en términos más pequeños.

2.- Modelo atómico de Thomson (1897)
Es una teoría la cual explicaba que el átomo esta compuesto por electrones con carga negativa en un átomo positivo.

3.- Modelo atómico de Rutherford (1911)
Habla sobre la estructura interna del átomo para explicar los resultados de su "experimento de la lámina de oro"

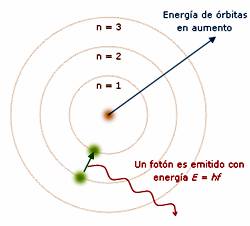
4.- Modelo átomico de Bohr (1913)
Es un modelo cuantificado del átomo que sirve para explicar cómo los electrones pueden tener órbitas estables alrededor del núcleo.
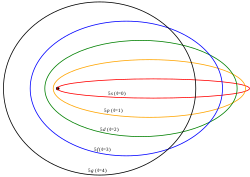
5.- Modelo átomico de Sommerfeld (1916)
Es el modelo de Bohr pero mejorado.
6.- Modelo átomico de Schrodinger
Es un modelo cuántico no relativista .

1.- Modelo atómico de John Dalton (1808)
Este modelo te explicaban como se combinaban las sustancias entre sí.
También te explicaba que aún habiendo distintos tipos de sustancias estas se podían explicar en términos más pequeños.
2.- Modelo atómico de Thomson (1897)
Es una teoría la cual explicaba que el átomo esta compuesto por electrones con carga negativa en un átomo positivo.

3.- Modelo atómico de Rutherford (1911)
Habla sobre la estructura interna del átomo para explicar los resultados de su "experimento de la lámina de oro"

4.- Modelo átomico de Bohr (1913)
Es un modelo cuantificado del átomo que sirve para explicar cómo los electrones pueden tener órbitas estables alrededor del núcleo.

5.- Modelo átomico de Sommerfeld (1916)
Es el modelo de Bohr pero mejorado.

6.- Modelo átomico de Schrodinger
Es un modelo cuántico no relativista .

viernes, 4 de marzo de 2016
Enlace químico
Los átomos se unen mediante los electrones más externos de la corteza atómica para alcanzar una situación de mayor estabilidad,como la de los gases nobles,cuya última capa está completa(con 8 electrones).
Según cómo se produzca la unión entre los átomos,existen tres tipos de enlaces:iónico,covalente y metálico.
Enlace iónico:

Enlace covalente
Según cómo se produzca la unión entre los átomos,existen tres tipos de enlaces:iónico,covalente y metálico.
Enlace iónico:
Enlace covalente
jueves, 3 de marzo de 2016
Moléculas,elementos y compuestos
Un elemento es una sustancia pura formada por átomos iguales.
Un compuesto es una sustancia pura formada por átomos de distintos elementos químicos y entre si en una relación numérica sencilla y constante,es decir,se puede en otros elementos.
1.- Nombre y símbolo de los elementos:
Actualmente se conocen 118 elementos,de los que unos 90 se encuentran en la naturaleza y el resto se han obtenido en el laboratorio. o aún no han sido aislados.
2.- Tabla periódica:
Los elementos están ordenados en una tabla periódica formada por 18 columnas,o grupos,y filas,o periodos.
Los elementos se pueden clasificar en :
1.- Metales: Situados a la izquierda de la tabla.Sus propiedades son: brillo, metálico, maleabilidad, ductilidad y conducción.
2.- No metales: Situados a la derecha,malos conductores de la electricidad.
3.- Semimetales o semiconductores: Situados entre los metales y los no metales.
4.- Radio atómico: El tamaño de un átomo.
5.- Energía de ionización: Expresa la energía necesaria para arrancar un electrón de la corteza atómica.
6.- Valencia: Es un número que indica la capacidad de un elemento para combinarse con otros elementos formando enlaces.
7.-
Un compuesto es una sustancia pura formada por átomos de distintos elementos químicos y entre si en una relación numérica sencilla y constante,es decir,se puede en otros elementos.
1.- Nombre y símbolo de los elementos:
Actualmente se conocen 118 elementos,de los que unos 90 se encuentran en la naturaleza y el resto se han obtenido en el laboratorio. o aún no han sido aislados.
2.- Tabla periódica:
Los elementos están ordenados en una tabla periódica formada por 18 columnas,o grupos,y filas,o periodos.
Los elementos se pueden clasificar en :
1.- Metales: Situados a la izquierda de la tabla.Sus propiedades son: brillo, metálico, maleabilidad, ductilidad y conducción.
2.- No metales: Situados a la derecha,malos conductores de la electricidad.
3.- Semimetales o semiconductores: Situados entre los metales y los no metales.
4.- Radio atómico: El tamaño de un átomo.
5.- Energía de ionización: Expresa la energía necesaria para arrancar un electrón de la corteza atómica.
6.- Valencia: Es un número que indica la capacidad de un elemento para combinarse con otros elementos formando enlaces.
7.-
miércoles, 2 de marzo de 2016
La estructura del átomo
El Átomo está divido en dos partes:
1.- El Núcleo: Se encuentran los protones y los neutrones que constituyen la mayor parte de la masa de todo el átomo.
2.- En la Corteza: Se encuentran los electrones orbitando alrededor del número.Los electrones tienen una masa 1000 veces más pequeña que la de los protones y neutrones.
Los números del átomo :
Z = nº de protones
A = nº de protones + nº de neutrones = nº de neutrones = A - Z
Los 118 elementos desconocidos se colocan ordenados por su número atómico en la llamada tabla periódica que veremos más adelante.
La masa del átomo depende principalmente del número de protones y de neutrones que lo formen.
El número másico (A) nos indica la cantidad de protones y neutrones que tiene el átomo.
A=Z+N
La distribución de los electrones :
Los electrones se dividen en capas o niveles de energía.
1.- El Núcleo: Se encuentran los protones y los neutrones que constituyen la mayor parte de la masa de todo el átomo.
2.- En la Corteza: Se encuentran los electrones orbitando alrededor del número.Los electrones tienen una masa 1000 veces más pequeña que la de los protones y neutrones.
Los números del átomo :
Z = nº de protones
A = nº de protones + nº de neutrones = nº de neutrones = A - Z
Los 118 elementos desconocidos se colocan ordenados por su número atómico en la llamada tabla periódica que veremos más adelante.
La masa del átomo depende principalmente del número de protones y de neutrones que lo formen.
El número másico (A) nos indica la cantidad de protones y neutrones que tiene el átomo.
A=Z+N
La distribución de los electrones :
Los electrones se dividen en capas o niveles de energía.
Sustancias puras y mezclas
Una sustancia es cada una de las diversas clases de de materia que existen en la naturaleza.Podemos clasificar las sustancias según la cantidad de elementos que contienen que nos encontramos a nuestro alrededor.
Sustancias puras:
Son sustancias constituidas por un único componente y propiedades físicas características.Algunas de estas propiedades son: La temperatura,el calor,la densidad,el sabor...
Mezclas:
Están compuestas por la unión de varias sustancias puras.Las sustancias conservan sus propiedades.
1.-Mezclas heterogéneas :
Algunas mezclas presentan un aspecto irregular y pueden distinguirse simple vista las distintas sustancias que las componen.
2.-Mezclas homogéneas o disoluciones
Algunas mezclas presentan un aspecto uniforme.Sus propiedades son las mismas en cualquiera de sus puntos y no podemos distinguir fácilmente las sustancias de las que están compuestas.
Sustancias puras:
Son sustancias constituidas por un único componente y propiedades físicas características.Algunas de estas propiedades son: La temperatura,el calor,la densidad,el sabor...
Mezclas:
Están compuestas por la unión de varias sustancias puras.Las sustancias conservan sus propiedades.
1.-Mezclas heterogéneas :
Algunas mezclas presentan un aspecto irregular y pueden distinguirse simple vista las distintas sustancias que las componen.
2.-Mezclas homogéneas o disoluciones
Algunas mezclas presentan un aspecto uniforme.Sus propiedades son las mismas en cualquiera de sus puntos y no podemos distinguir fácilmente las sustancias de las que están compuestas.
Suscribirse a:
Entradas (Atom)


